Tag: Ema
Farmaci anti diabete e obesità, allarme dell’Ema: boom di prodotti illegali
L'Agenzia europea dei medicinali ha registrato negli ultimi mesi un forte aumento di medicinali illegali, venduti online, a base di semaglutide, liraglutide e tirzepatide (i famosi Ozempic & Co.), utilizzati per perdere peso e curare il diabete. L'Ema avverte sui gravi rischi per la salute
Azitromicina, stretta sull’uso dell’antibiotico in Europa
Negli ultimi anni è aumentata l'antibiotico resistenza verso l'azitromicina, uno dei farmaci più utilizzati sia nei bambini che negli adulti. Il rischio è che diventi un'arma spuntata, per questo l'Ema chiede di non prescriverlo più in alcuni casi, come la cura dell'acne e dell'asma
Farmaci generici, l’Ue ne sospende 400 testati in India. Ecco quelli...
La Commissione Europea ha sospeso le autorizzazioni all'immissione in commercio di circa 400 farmaci generici testati dalla società indiana Synapse Labs a causa di prove insufficienti sull'affidabilità dei dati sperimentali
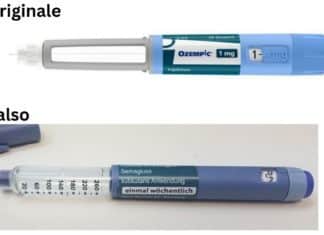
Allerta Ema: in circolazione falso Ozempic, medicinale contro il diabete
L'Agenzia europea del farmaco, informata dall'autorithy tedesca, segnala la presenza di penne falsamente etichettate come il medicinale per il diabete Ozempic
Farmaci per il trattamento dei tumori: si esagera con le indicazioni...
I farmaci dopo una prima autorizzazione sulla base di dossier vedono spesso ampliarsi le indicazioni d'uso, il che significa maggiore redditività per Big Pharma. Ma uno studio scientifico sui medicinali per la cura dei tumori mette in luce che spesso i benefici diminuiscono man mano che aumentano le indicazioni.
“Rischio suicidio”: Ema indaga sui farmaci per dimagrire
L'Agenzia europea del farmaco sta conducendo una revisione sui farmaci per dimagrire come il Wegovy, Saxenda e Ozempic: il sospetto è un possibile collegamento con un aumento del rischio di suicidio, dopo tre casi registrati in Islanda
Fluorochinoloni, richiamo di Ema ai medici: “Basta prescrizione facili, si rischiano...
Ancora un richiamo da parte dell'Agenzia europea per i medicinali nei confronti dei medici che con troppa facilità prescrivono antibiotici della famiglia dei fluorochinolonici, che possono avere effetti collaterali invalidanti
Possibile collegamento con cancro: Ema avvia revisione dell’idrossiprogesterone, farmaco per prevenire...
L'Autorità europea per i medicinali (Ema) ha avviato una revisione dei medicinali contenenti idrossiprogesterone a seguito delle preoccupazioni circa la sicurezza e l'efficacia di questi medicinali, e della possibilità di maggiori rischio di cancro.
Fluorochinoloni, la denuncia: in Italia ogni mese 200mila prescrizioni non corrette
"La prescrizione sconsiderata di fluorochinoloni avviene in Italia come in Francia, ma peggio. Genera un gran numero di persone danneggiate e morti per pura negligenza dei medici e delle autorità mediche". La dura accusa arriva da Philippe Coville, presidente dell'Associazione francese d'aiuto e informazione sugli effetti deleteri dei fluorochinoloni
Biossido di titanio: ecco dove non lo troverete più (e dove...
Da oggi il biossido di titanio scomparirà da molti alimenti (gomme, zuppe e dolciumi) ma continueremo a trovarlo in tanti altri prodotti...come i farmaci
Biossido di titanio, l’Ema frena: è difficile sostituirlo nei farmaci
Secondo l'Agenzia dei farmaci europea, nessuno dei sostituti attualmente presenti sul mercato ha le caratteristiche tali da poter essere un valido sostituto del biossido di titanio. Inoltre, l'Agenzia sottolinea che il processo di sostitutizione potrebbe durare anche 10 anni dal momento che la riformulazione richiede numerosi controlli (stabilità, scioglimento, non interferenza con altri componenti, ecc.) e che ogni nuovo farmaco dovrà essere rivalutato dalle autorità nazionali e da se stesso
Cosa hanno detto Ema e Aifa sui rischi di Astrazeneca per...
A fronte di una rassicurazione complessiva sul vaccino AstraZeneca, che infatti riparte nei centri vaccinazione italiani, rimangono alcune possibili connessioni tra patologie e effetti collaterali gravi per i quali la stessa Agenzia europea del farmaco ha assicurato un supplemento di approfondimento.