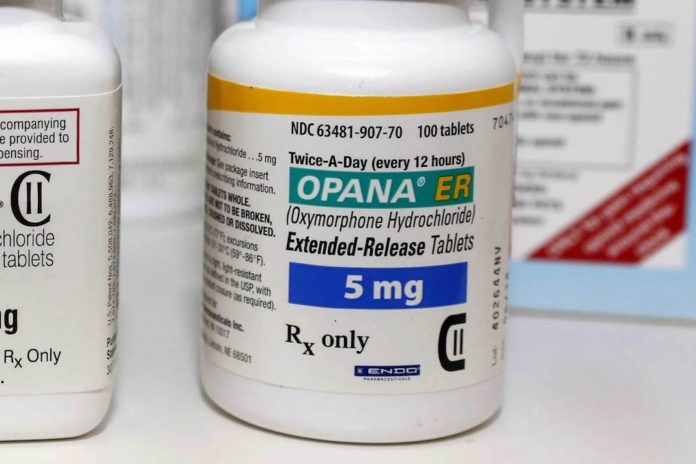
La Food and Drug Administration ha chiesto alla Endo Pharmaceuticals, il produttore di Opana ER, un antidolorifico oppioide semi-sintetico a rilascio estratto, di rimuovere il farmaco dal mercato. L’agenzia ha concluso che gli effeti legati all’abuso del farmaco superano di gran lunga il suo valore terapeutico. È quanto rivela Consumer Reports, l’associazione più importante dei consumatori statunitensi.
Endo aveva riformulato l’Opana ER (ossimorfone cloridrato, presente anche in Italia) per rendere più difficile l’abuso, ma la Fda ha determinato che questo cambiamento ha portato in ultima analisi a “uno spostamento significativo dei casi di abuso di Opana ER dall’uso nasale alle iniezioni”.
Il cloridrato dell’Oxymorphone è noto per gli effetti molto forti quando è macinato, mescolato con acqua e iniettato. Ha un’emivita breve, il che significa che gli effetti stuoefacenti arrivano prima che con altri oppioidi.
La FDA ha collegato il cambio di formulazione dell’Opana con un aumento di casi di HIV e all’epatite C (dovuti all’uso di siringhe non sterili), così come a casi di microangiopatia trombotica.
“Quando abbiamo determinato che il prodotto aveva pericolose conseguenze non intenzionali, abbiamo deciso di chiedere il suo ritiro dal mercato”, ha dichiarato Janet Woodcock, M.D., direttore del Centro di valutazione e ricerca di farmaci della FDA. “Questa azione proteggerà il pubblico da ulteriori potenziali abusi e abusi di questo prodotto”.
L’Opana è stato collegato all’epidemia di HIV del 2015 nella comunità rurale indiana di Austin che ha portato a decine di casi HIV confermati in una città di sole 4.000 persone. Un incidente così grave che il governatore Mike Pence ha dichiarato un’emergenza sanitaria pubblica.
La società dice che sta “valutando l’intera gamma delle opzioni potenziali per scegliere il percorso appropriato di intervento”.










